Atom ve Atom Modelleri Nelerdir?
Atom ve Atom Modelleri Nelerdir?
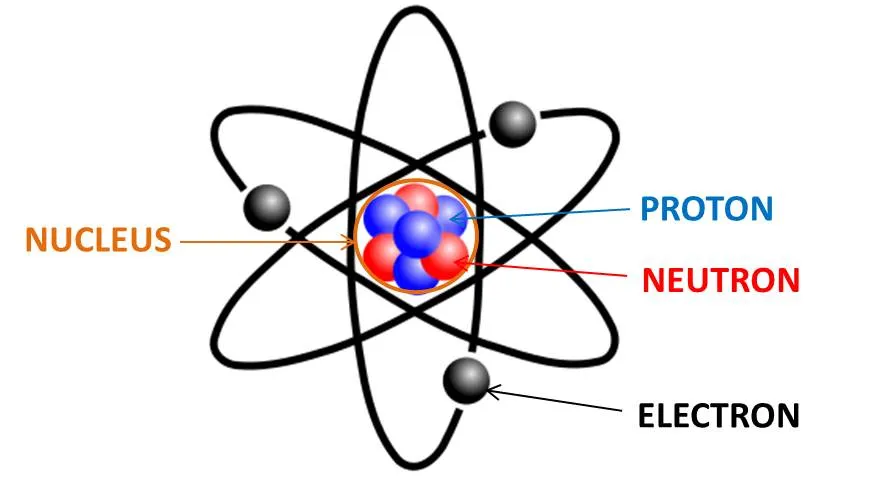
Atom, maddenin en küçük yapı taşıdır. Atomlar, çekirdek ve çekirdeğin etrafında dönen elektronlardan oluşur. Çekirdek, proton ve nötron adı verilen iki tür parçacıktan meydana gelir. Protonlar, atomun pozitif yükünü taşırken, nötronlar yüksüz kalır. Elektronlar ise atomun negatif yükünü taşır.
Atom modelleri, atomun yapısını ve özelliklerini açıklamak için geliştirilen teorik tasarımlardır. Atom modelleri, bilimsel araştırmalar ve deneyler sonucunda zaman içinde değişiklik göstermiştir. Atom modellerinin gelişimi, atom fiziği ve kimyanın temelini oluşturur.
Atom modellerinin tarihsel gelişimine bakacak olursak, şu şekilde bir sıralama yapabiliriz:
- Demokritos Modeli: Antik Yunan filozofu Demokritos, MÖ 5. yüzyılda atom kavramını ortaya atmıştır. Demokritos'a göre, madde boşlukla dolu küçük parçacıklardan oluşur. Bu parçacıklar bölünemez, değişmez ve farklı şekil ve büyüklüklere sahiptir. Bu modelde, atomun iç yapısı hakkında herhangi bir bilgi yoktur.
- Dalton Modeli: İngiliz kimyacı John Dalton, 1808 yılında atom teorisini geliştirmiştir. Dalton'a göre, her element farklı atomlardan oluşur. Atomlar bölünemez, değişmez ve aynı elementin atomları birbirine eşittir. Farklı elementlerin atomları ise farklı kütlelere sahiptir. Bu modelde de atomun iç yapısı hakkında herhangi bir bilgi yoktur.
- Thomson Modeli: İngiliz fizikçi Joseph John Thomson, 1897 yılında elektronu keşfetmiştir. Thomson'a göre, atom pozitif yüklü bir küredir ve içinde negatif yüklü elektronlar yer alır. Bu modele göre, atom elektriksel olarak nötrdür ve elektronların sayısı protonların sayısına eşittir. Bu model, karpuz modeli veya üzüm keki modeli olarak da adlandırılır.
- Rutherford Modeli: Yeni Zelandalı fizikçi Ernest Rutherford, 1911 yılında altın levha deneyini yapmıştır. Bu deneyde, Rutherford alfa parçacıklarını altın levhaya çarptırmış ve bunların bir kısmının geri saçıldığını gözlemlemiştir. Bu sonuçtan yola çıkarak, Rutherford atomun çekirdekli bir yapı olduğunu ileri sürmüştür. Rutherford'a göre, atomun büyük bir kısmı boşluktan oluşur ve çekirdek çok küçük ama çok yoğundur. Çekirdek pozitif yüklüdür ve protonları içerir. Elektronlar ise çekirdeğin etrafında dairesel yörüngelerde dönerler.
- Bohr Modeli: Danimarkalı fizikçi Niels Bohr, 1913 yılında hidrojen atomunun yapısını açıklamak için bir model önermiştir. Bohr'a göre, elektronlar belirli enerji seviyelerine sahip yörüngelerde dönerler. Elektronlar enerji seviyeleri arasında geçiş yapabilirler ancak ara değerler alamazlar. Elektronlar daha düşük enerjili yörüngelere geçtiklerinde ışık yayınlarlar. Bu model hidrojen gibi tek elektronlu atomlar için iyi sonuç verir ancak çok elektronlu atomlar için yetersiz kalır.
- Sommerfeld Modeli: Alman fizikçi Arnold Sommerfeld, 1916 yılında Bohr modelini genelleştirmiştir. Sommerfeld'a göre, elektronlar eliptik yörüngelerde dönerler ve yörüngelerin şekli elektronların hızına bağlıdır. Bu model, atom spektrumlarını daha iyi açıklar ancak elektronların birbirleriyle etkileşimini göz ardı eder.
- Schrödinger Modeli: Avusturyalı fizikçi Erwin Schrödinger, 1926 yılında atomun kuantum mekaniği ile açıklanabileceğini göstermiştir. Schrödinger'a göre, elektronlar belirli olasılıklarla bulunabilecekleri bölgelerdir. Bu bölgeler, atomun orbitalleri olarak adlandırılır. Orbitallerin şekli ve enerjisi, Schrödinger denkleminin çözümü ile bulunur. Bu model, atomun dalga-parçacık ikiliği olarak tanımlanır.
- Modern Atom Modeli: Modern atom modeli, Schrödinger modelinin geliştirilmiş halidir. Bu modelde, atomun çekirdeği proton ve nötronlardan oluşur. Proton ve nötronlar da kuark adı verilen daha küçük parçacıklardan meydana gelir. Elektronlar ise orbitallerde bulunurlar. Orbitallerin şekli ve enerjisi, kuantum sayıları ile belirlenir. Kuantum sayıları, elektronların ana enerji seviyesini, orbital şeklini, orbital yönelimini ve elektron spinini ifade eder. Bu model, atomun en güncel ve en doğru modelidir.






